Η μελέτη των διεργασιών που συμβαίνουν στα στατιστικά συστήματα περιπλέκεται από το ελάχιστο μέγεθος των σωματιδίων και τον τεράστιο αριθμό τους. Είναι πρακτικά αδύνατο να εξεταστεί κάθε σωματίδιο ξεχωριστά, επομένως, εισάγονται στατιστικές ποσότητες: η μέση ταχύτητα των σωματιδίων, η συγκέντρωσή τους, η μάζα σωματιδίων. Ο τύπος που χαρακτηρίζει την κατάσταση του συστήματος, λαμβάνοντας υπόψη τις μικροσκοπικές παραμέτρους, ονομάζεται η βασική εξίσωση της μοριακής-κινητικής θεωρίας των αερίων (MKT).
Λίγα για τη μέση ταχύτητα σωματιδίων
Ο προσδιορισμός της ταχύτητας των σωματιδίων πραγματοποιήθηκε αρχικά πειραματικά. Ένα πολύ γνωστό πείραμα από το σχολικό πρόγραμμα σπουδών, που διεξήχθη από τον Otto Stern, κατέστησε δυνατή τη δημιουργία μιας ιδέας για τις ταχύτητες των σωματιδίων. Κατά τη διάρκεια του πειράματος, μελετήθηκε η κίνηση των ατόμων αργύρου σε περιστρεφόμενους κυλίνδρους: πρώτα, σε ακίνητη κατάσταση της εγκατάστασης, μετά όταν περιστρεφόταν με μια ορισμένη γωνιακή ταχύτητα.
Ως αποτέλεσμα, διαπιστώθηκε ότι η ταχύτητα των μορίων του αργύρου υπερβαίνει την ταχύτητα του ήχου και είναι 500 m/s. Το γεγονός είναι αρκετά ενδιαφέρον, αφού είναι δύσκολο για ένα άτομο να αισθανθεί τέτοιες ταχύτητες κίνησης σωματιδίων σε ουσίες.
Ιδανικό αέριο
Συνεχίστε την έρευναΦαίνεται δυνατό μόνο σε ένα σύστημα του οποίου οι παράμετροι μπορούν να προσδιοριστούν με άμεσες μετρήσεις χρησιμοποιώντας φυσικά όργανα. Η ταχύτητα μετριέται με ταχύμετρο, αλλά η ιδέα της προσάρτησης ενός ταχύμετρου σε ένα μόνο σωματίδιο είναι παράλογη. Μόνο μια μακροσκοπική παράμετρος που σχετίζεται με την κίνηση των σωματιδίων μπορεί να μετρηθεί απευθείας.
Εξετάστε την πίεση αερίου. Η πίεση στα τοιχώματα του δοχείου δημιουργείται από τις κρούσεις των μορίων του αερίου στο δοχείο. Η ιδιαιτερότητα της αέριας κατάστασης της ύλης είναι σε αρκετά μεγάλες αποστάσεις μεταξύ των σωματιδίων και στη μικρή τους αλληλεπίδραση μεταξύ τους. Αυτό σας επιτρέπει να μετρήσετε απευθείας την πίεσή του.
Οποιοδήποτε σύστημα αλληλεπιδρώντων σωμάτων χαρακτηρίζεται από δυναμική ενέργεια και κινητική ενέργεια κίνησης. Το πραγματικό αέριο είναι ένα πολύπλοκο σύστημα. Η μεταβλητότητα της δυναμικής ενέργειας δεν προσφέρεται για συστηματοποίηση. Το πρόβλημα μπορεί να λυθεί με την εισαγωγή ενός μοντέλου που φέρει τις χαρακτηριστικές ιδιότητες του αερίου, παραμερίζοντας την πολυπλοκότητα της αλληλεπίδρασης.
Ιδανικό αέριο είναι μια κατάσταση της ύλης στην οποία η αλληλεπίδραση των σωματιδίων είναι αμελητέα, η δυναμική ενέργεια της αλληλεπίδρασης τείνει στο μηδέν. Μόνο η ενέργεια της κίνησης, η οποία εξαρτάται από την ταχύτητα των σωματιδίων, μπορεί να θεωρηθεί σημαντική.
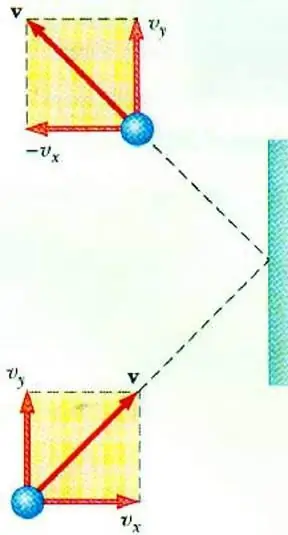
Ιδανική πίεση αερίου
Για να αποκαλυφθεί η σχέση μεταξύ της πίεσης του αερίου και της ταχύτητας των σωματιδίων του επιτρέπει τη βασική εξίσωση του MKT ενός ιδανικού αερίου. Ένα σωματίδιο που κινείται σε ένα δοχείο, κατά την πρόσκρουση με τον τοίχο, μεταφέρει σε αυτό μια ώθηση, η τιμή της οποίας μπορεί να προσδιοριστεί με βάση τον δεύτερο νόμοNewton:
F∆t=2m0vx
Η μεταβολή της ορμής ενός σωματιδίου κατά την ελαστική κρούση σχετίζεται με μια αλλαγή στην οριζόντια συνιστώσα της ταχύτητάς του. F είναι η δύναμη που ασκείται από την πλευρά του σωματιδίου στον τοίχο για μικρό χρονικό διάστημα t. m0 - μάζα σωματιδίων.
Όλα τα σωματίδια αερίου συγκρούονται με την επιφάνεια της περιοχής S κατά τη διάρκεια του χρόνου Δt, κινούνται προς την κατεύθυνση της επιφάνειας με ταχύτητα vx και βρίσκονται σε έναν κύλινδρο όγκου Sυ x Δt. Στη συγκέντρωση σωματιδίων n, ακριβώς τα μισά μόρια κινούνται προς το τοίχωμα, τα άλλα μισά κινούνται προς την αντίθετη κατεύθυνση.
Έχοντας εξετάσει τη σύγκρουση όλων των σωματιδίων, μπορούμε να γράψουμε το νόμο του Νεύτωνα για τη δύναμη που ασκείται στην περιοχή:
F∆t=nm0vx2S∆t
Δεδομένου ότι η πίεση αερίου ορίζεται ως ο λόγος της δύναμης που ενεργεί κάθετα στην επιφάνεια προς την περιοχή της τελευταίας, μπορούμε να γράψουμε:
p=F: S=nm0vx2
Η σχέση που προκύπτει ως η βασική εξίσωση του MKT δεν μπορεί να περιγράψει ολόκληρο το σύστημα, αφού λαμβάνεται υπόψη μόνο μία κατεύθυνση κίνησης.
Διανομή Maxwell
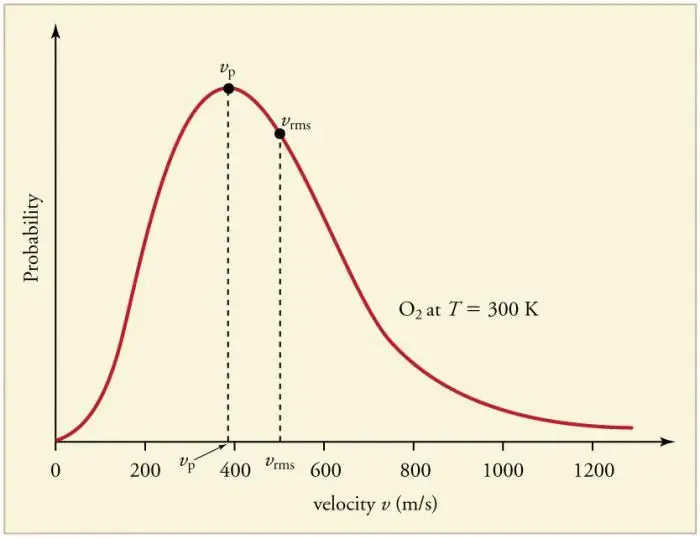
Συνεχείς συχνές συγκρούσεις σωματιδίων αερίου με τα τοιχώματα και μεταξύ τους οδηγούν στην καθιέρωση μιας ορισμένης στατιστικής κατανομής των σωματιδίων ως προς τις ταχύτητες (ενέργειες). Οι κατευθύνσεις όλων των διανυσμάτων ταχύτητας αποδεικνύονται εξίσου πιθανές. Αυτή η κατανομή ονομάζεται κατανομή Maxwell. Το 1860 αυτό το μοτίβο ήτανπροέρχεται από τον J. Maxwell με βάση το MKT. Οι κύριες παράμετροι του νόμου κατανομής ονομάζονται ταχύτητες: πιθανές, που αντιστοιχούν στη μέγιστη τιμή της καμπύλης, και ρίζα μέσου τετραγώνου vkv=√‹v2 › - το μέσο τετράγωνο της ταχύτητας των σωματιδίων.
Η αύξηση της θερμοκρασίας του αερίου αντιστοιχεί σε αύξηση της ταχύτητας.
Με βάση το γεγονός ότι όλες οι ταχύτητες είναι ίσες και οι μονάδες τους έχουν την ίδια τιμή, μπορούμε να υποθέσουμε:
‹v2›=‹vx2› + ‹v y2› + ‹vz2›, από: ‹ vx2›=‹v2›: 3
Η βασική εξίσωση του MKT, λαμβάνοντας υπόψη τη μέση τιμή της πίεσης του αερίου, είναι:
p=nm0‹v2›: 3.
Αυτή η σχέση είναι μοναδική στο ότι καθορίζει τη σχέση μεταξύ μικροσκοπικών παραμέτρων: ταχύτητα, μάζα σωματιδίων, συγκέντρωση σωματιδίων και πίεση αερίου γενικά.
Χρησιμοποιώντας την έννοια της κινητικής ενέργειας των σωματιδίων, η βασική εξίσωση του MKT μπορεί να ξαναγραφτεί διαφορετικά:
p=2nm0‹v2›: 6=2n‹Ek›: 3
Η πίεση ενός αερίου είναι ανάλογη με τη μέση τιμή της κινητικής ενέργειας των σωματιδίων του.
Θερμοκρασία
Είναι ενδιαφέρον ότι για μια σταθερή ποσότητα αερίου σε ένα κλειστό δοχείο, μπορεί κανείς να συσχετίσει την πίεση του αερίου και τη μέση τιμή της ενέργειας κίνησης των σωματιδίων. Σε αυτή την περίπτωση, η πίεση μπορεί να μετρηθεί με τη μέτρηση της ενέργειαςσωματίδια.
Τι να κάνετε; Ποια τιμή μπορεί να συγκριθεί με την κινητική ενέργεια; Η θερμοκρασία αποδεικνύεται ότι είναι μια τέτοια τιμή.

Η θερμοκρασία είναι ένα μέτρο της θερμικής κατάστασης των ουσιών. Για τη μέτρησή του, χρησιμοποιείται ένα θερμόμετρο, η βάση του οποίου είναι η θερμική διαστολή του ρευστού εργασίας (οινόπνευμα, υδράργυρος) όταν θερμαίνεται. Η κλίμακα του θερμομέτρου δημιουργείται πειραματικά. Συνήθως, τοποθετούνται σημάδια σε αυτό που αντιστοιχούν στη θέση του ρευστού εργασίας κατά τη διάρκεια κάποιας φυσικής διαδικασίας που συμβαίνει σε σταθερή θερμική κατάσταση (βραστό νερό, λιώσιμο πάγου). Διαφορετικά θερμόμετρα έχουν διαφορετικές κλίμακες. Για παράδειγμα, Κελσίου, Φαρενάιτ.

Παγκόσμια κλίμακα θερμοκρασίας
Τα θερμόμετρα αερίου μπορούν να θεωρηθούν πιο ενδιαφέροντα όσον αφορά την ανεξαρτησία από τις ιδιότητες του ρευστού εργασίας. Η κλίμακα τους δεν εξαρτάται από τον τύπο του αερίου που χρησιμοποιείται. Σε μια τέτοια συσκευή, μπορεί κανείς να ξεχωρίσει υποθετικά τη θερμοκρασία στην οποία η πίεση του αερίου τείνει στο μηδέν. Οι υπολογισμοί δείχνουν ότι αυτή η τιμή αντιστοιχεί σε -273,15 oC. Η κλίμακα θερμοκρασίας (κλίμακα απόλυτης θερμοκρασίας ή κλίμακα Kelvin) εισήχθη το 1848. Ως κύριο σημείο αυτής της κλίμακας λήφθηκε η πιθανή θερμοκρασία μηδενικής πίεσης αερίου. Ένα τμήμα μονάδας της κλίμακας ισούται με μια μοναδιαία τιμή της κλίμακας Κελσίου. Φαίνεται πιο βολικό να γράψετε τη βασική εξίσωση MKT χρησιμοποιώντας τη θερμοκρασία κατά τη μελέτη διεργασιών αερίου.
Σχέση μεταξύ πίεσης και θερμοκρασίας
Εμπειρικά, μπορείτε να το επιβεβαιώσετεαναλογία της πίεσης του αερίου προς τη θερμοκρασία του. Ταυτόχρονα, διαπιστώθηκε ότι η πίεση είναι ευθέως ανάλογη με τη συγκέντρωση των σωματιδίων:
P=nkT,
όπου T είναι απόλυτη θερμοκρασία, το k είναι μια σταθερά ίση με 1,38•10-23J/K.
Η θεμελιώδης τιμή, η οποία έχει σταθερή τιμή για όλα τα αέρια, ονομάζεται σταθερά Boltzmann.
Συγκρίνοντας την εξάρτηση της πίεσης από τη θερμοκρασία και τη βασική εξίσωση των αερίων MKT, μπορούμε να γράψουμε:
‹Ek›=3kT: 2
Η μέση τιμή της κινητικής ενέργειας της κίνησης των μορίων αερίου είναι ανάλογη της θερμοκρασίας του. Δηλαδή, η θερμοκρασία μπορεί να χρησιμεύσει ως μέτρο της κινητικής ενέργειας της κίνησης των σωματιδίων.






