Κάθε άτομο κατά τη διάρκεια της ζωής του συναντά σώματα που βρίσκονται σε μία από τις τρεις αθροιστικές καταστάσεις της ύλης. Η απλούστερη κατάσταση συσσωμάτωσης για μελέτη είναι το αέριο. Στο άρθρο, θα εξετάσουμε την έννοια του ιδανικού αερίου, θα δώσουμε την εξίσωση της κατάστασης του συστήματος και θα δώσουμε επίσης κάποια προσοχή στην περιγραφή της απόλυτης θερμοκρασίας.
Αέρια κατάσταση της ύλης
Κάθε μαθητής έχει μια καλή ιδέα για την κατάσταση της ύλης που μιλά όταν ακούει τη λέξη "αέριο". Αυτή η λέξη νοείται ως ένα σώμα που είναι ικανό να καταλάβει οποιονδήποτε όγκο του παρέχεται. Δεν είναι σε θέση να διατηρήσει το σχήμα του, γιατί δεν μπορεί να αντισταθεί ούτε στην παραμικρή εξωτερική επιρροή. Επίσης, το αέριο δεν διατηρεί όγκο, κάτι που το διακρίνει όχι μόνο από τα στερεά, αλλά και από τα υγρά.
Όπως ένα υγρό, ένα αέριο είναι μια ρευστή ουσία. Στη διαδικασία κίνησης των στερεών σωμάτων σε αέρια, τα τελευταία εμποδίζουν αυτή την κίνηση. Η δύναμη που προκύπτει ονομάζεται αντίσταση. Η αξία του εξαρτάται απόταχύτητα του σώματος στο αέριο.
Ισχυρά παραδείγματα αερίων είναι ο αέρας, το φυσικό αέριο που χρησιμοποιείται για τη θέρμανση των σπιτιών και το μαγείρεμα, τα αδρανή αέρια (Ne, Ar) που χρησιμοποιούνται για την πλήρωση διαφημιστικών σωλήνων λάμψης ή για τη δημιουργία ενός αδρανούς (μη επιθετικού, προστατευτικού) περιβάλλοντος κατά τη συγκόλληση.
Ιδανικό αέριο
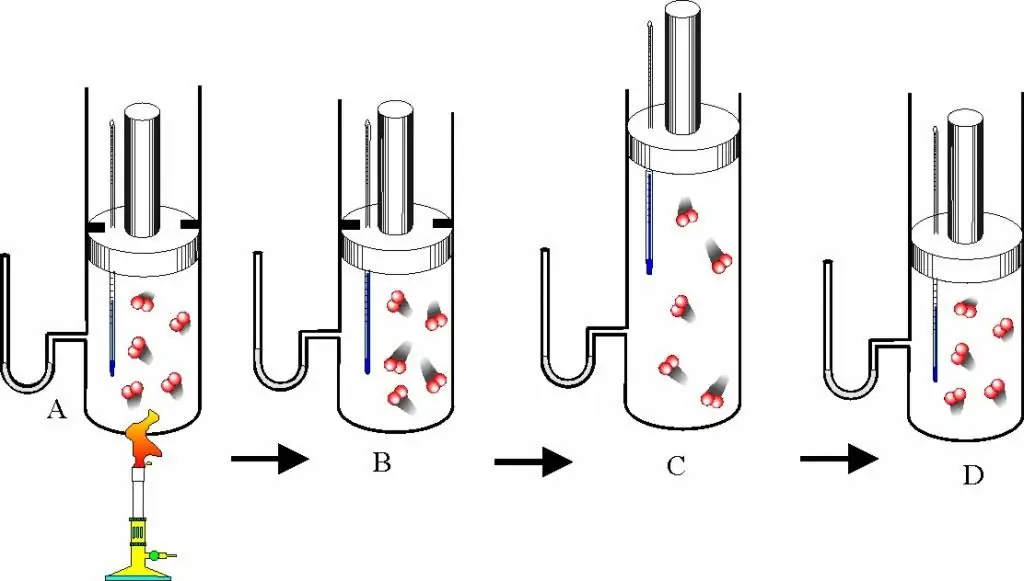
Πριν προχωρήσετε στην περιγραφή των νόμων των αερίων και της εξίσωσης κατάστασης, θα πρέπει να κατανοήσετε καλά το ερώτημα του τι είναι ιδανικό αέριο. Αυτή η έννοια εισάγεται στη μοριακή κινητική θεωρία (MKT). Ιδανικό αέριο είναι κάθε αέριο που ικανοποιεί τα ακόλουθα χαρακτηριστικά:
- Τα σωματίδια που το σχηματίζουν δεν αλληλεπιδρούν μεταξύ τους εκτός από άμεσες μηχανικές συγκρούσεις.
- Σαν αποτέλεσμα της σύγκρουσης των σωματιδίων με τα τοιχώματα του σκάφους ή μεταξύ τους, διατηρείται η κινητική τους ενέργεια και η ορμή τους, δηλαδή η σύγκρουση θεωρείται απολύτως ελαστική.
- Τα σωματίδια δεν έχουν διαστάσεις, αλλά έχουν πεπερασμένη μάζα, δηλαδή μοιάζουν με υλικά σημεία.
Είναι φυσικό ότι οποιοδήποτε αέριο δεν είναι ιδανικό, αλλά πραγματικό. Ωστόσο, για την επίλυση πολλών πρακτικών προβλημάτων, αυτές οι προσεγγίσεις είναι αρκετά έγκυρες και μπορούν να χρησιμοποιηθούν. Υπάρχει ένας γενικός εμπειρικός κανόνας που λέει: ανεξάρτητα από τη χημική φύση, εάν ένα αέριο έχει θερμοκρασία πάνω από τη θερμοκρασία δωματίου και πίεση της τάξης της ατμοσφαιρικής ή χαμηλότερη, τότε μπορεί να θεωρηθεί ιδανικό με υψηλή ακρίβεια και μπορεί να χρησιμοποιηθεί για να περιγράψει το.τύπος της εξίσωσης ιδανικού αερίου κατάστασης.
νόμος Clapeyron-Mendeleev
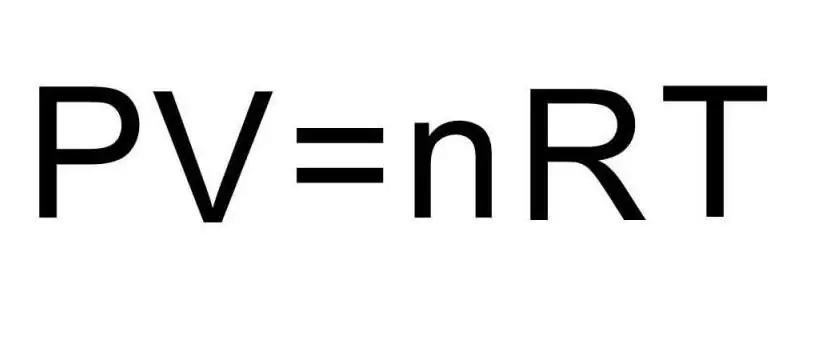
Οι μεταβάσεις μεταξύ διαφορετικών συνολικών καταστάσεων της ύλης και διεργασιών σε μια ενιαία αθροιστική κατάσταση αντιμετωπίζονται από τη θερμοδυναμική. Η πίεση, η θερμοκρασία και ο όγκος είναι τρεις ποσότητες που καθορίζουν μοναδικά οποιαδήποτε κατάσταση ενός θερμοδυναμικού συστήματος. Ο τύπος για την εξίσωση της κατάστασης ενός ιδανικού αερίου συνδυάζει και τις τρεις αυτές ποσότητες σε μια ενιαία ισότητα. Ας γράψουμε αυτόν τον τύπο:
PV=nRT
Εδώ P, V, T - πίεση, όγκος, θερμοκρασία, αντίστοιχα. Η τιμή του n είναι η ποσότητα της ουσίας σε mol, και το σύμβολο R υποδηλώνει την καθολική σταθερά των αερίων. Αυτή η ισότητα δείχνει ότι όσο μεγαλύτερο είναι το γινόμενο της πίεσης και του όγκου, τόσο μεγαλύτερο πρέπει να είναι το γινόμενο της ποσότητας της ουσίας και της θερμοκρασίας.

Ο τύπος για την εξίσωση της κατάστασης ενός αερίου ονομάζεται νόμος Clapeyron-Mendeleev. Το 1834, ο Γάλλος επιστήμονας Emile Clapeyron, συνοψίζοντας τα πειραματικά αποτελέσματα των προκατόχων του, κατέληξε σε αυτή την εξίσωση. Ωστόσο, ο Clapeyron χρησιμοποίησε έναν αριθμό σταθερών, τις οποίες ο Mendeleev αντικατέστησε αργότερα με μία - την καθολική σταθερά αερίου R (8, 314 J / (molK)). Επομένως, στη σύγχρονη φυσική, αυτή η εξίσωση πήρε το όνομά της από τα ονόματα Γάλλων και Ρώσων επιστημόνων.

Άλλες μορφές εξισώσεων
Παραπάνω, γράψαμε την εξίσωση κατάστασης Mendeleev-Clapeyron για ένα ιδανικό αέριο στο γενικά αποδεκτό καιβολική μορφή. Ωστόσο, σε προβλήματα στη θερμοδυναμική, μπορεί συχνά να απαιτείται μια ελαφρώς διαφορετική μορφή. Τρεις ακόμη τύποι γράφονται παρακάτω, οι οποίοι προκύπτουν άμεσα από τη γραπτή εξίσωση:
PV=NkBT;
PV=m/MRT;
P=ρRT/M.
Αυτές οι τρεις εξισώσεις είναι επίσης καθολικές για ένα ιδανικό αέριο, μόνο σε αυτές εμφανίζονται ποσότητες όπως η μάζα m, η μοριακή μάζα M, η πυκνότητα ρ και ο αριθμός των σωματιδίων N που αποτελούν το σύστημα. Το σύμβολο kB εδώ υποδηλώνει τη σταθερά Boltzmann (1, 3810-23J/K).
Νόμος Boyle-Mariotte
Όταν ο Clapeyron συνέταξε την εξίσωσή του, βασίστηκε σε νόμους αερίων που είχαν ανακαλυφθεί πειραματικά αρκετές δεκαετίες νωρίτερα. Ένα από αυτά είναι ο νόμος Boyle-Mariotte. Αντανακλά μια ισοθερμική διαδικασία σε ένα κλειστό σύστημα, ως αποτέλεσμα της οποίας μεταβάλλονται μακροσκοπικές παράμετροι όπως η πίεση και ο όγκος. Αν βάλουμε T και n σταθερά στην εξίσωση της κατάστασης για ένα ιδανικό αέριο, τότε ο νόμος του αερίου θα πάρει τη μορφή:
P1V1=P2V 2
Αυτός είναι ο νόμος Boyle-Mariotte, ο οποίος λέει ότι το γινόμενο της πίεσης και του όγκου διατηρείται κατά τη διάρκεια μιας αυθαίρετης ισοθερμικής διαδικασίας. Σε αυτήν την περίπτωση, οι ίδιες οι τιμές P και V αλλάζουν.
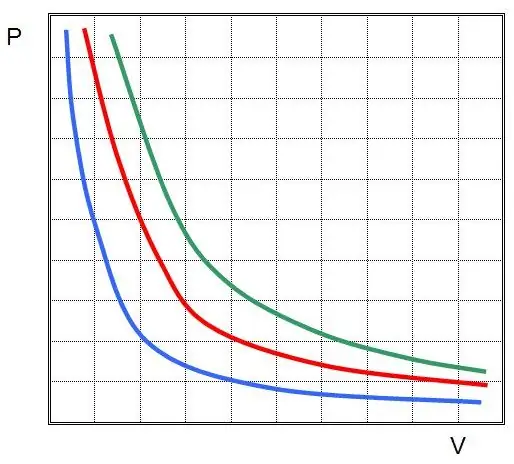
Αν σχεδιάσετε P(V) ή V(P), τότε οι ισόθερμες θα είναι υπερβολές.
Οι νόμοι του Charles και του Gay-Lussac
Αυτοί οι νόμοι περιγράφουν μαθηματικά το ισοβαρικό και το ισοχωρικόδιεργασίες, δηλαδή τέτοιες μεταβάσεις μεταξύ των καταστάσεων του συστήματος αερίων, στις οποίες διατηρείται η πίεση και ο όγκος, αντίστοιχα. Ο νόμος του Καρόλου μπορεί να γραφτεί μαθηματικά ως εξής:
V/T=const όταν n, P=const.
Ο νόμος του Gay-Lussac είναι γραμμένος ως εξής:
P/T=const όταν n, V=const.
Αν και οι δύο ισότητες παρουσιάζονται με τη μορφή γραφήματος, τότε θα λάβουμε ευθείες γραμμές που έχουν κλίση σε κάποια γωνία ως προς τον άξονα x. Αυτός ο τύπος γραφήματος υποδεικνύει μια άμεση αναλογία μεταξύ όγκου και θερμοκρασίας σε σταθερή πίεση και μεταξύ πίεσης και θερμοκρασίας σε σταθερό όγκο.
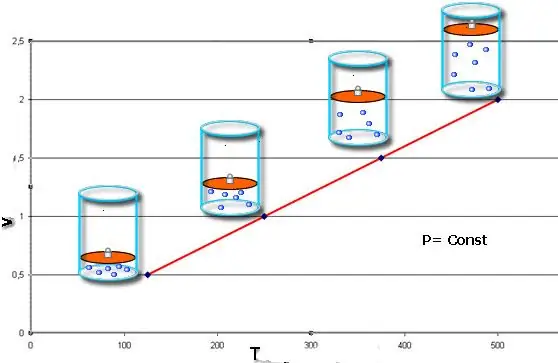
Σημειώστε ότι και οι τρεις εξεταζόμενοι νόμοι αερίων δεν λαμβάνουν υπόψη τη χημική σύσταση του αερίου, καθώς και την αλλαγή στην ποσότητα της ύλης του.
Απόλυτη θερμοκρασία
Στην καθημερινή ζωή, έχουμε συνηθίσει να χρησιμοποιούμε την κλίμακα θερμοκρασίας Κελσίου, καθώς είναι βολική για την περιγραφή των διεργασιών γύρω μας. Έτσι, το νερό βράζει στους 100 oC και παγώνει στους 0 oC. Στη φυσική, αυτή η κλίμακα αποδεικνύεται άβολη, επομένως, χρησιμοποιείται η λεγόμενη κλίμακα απόλυτης θερμοκρασίας, η οποία εισήχθη από τον Λόρδο Κέλβιν στα μέσα του 19ου αιώνα. Σύμφωνα με αυτήν την κλίμακα, η θερμοκρασία μετριέται σε Kelvin (K).
Πιστεύεται ότι σε θερμοκρασία -273, 15 oC δεν υπάρχουν θερμικές δονήσεις ατόμων και μορίων, η κίνησή τους προς τα εμπρός σταματά εντελώς. Αυτή η θερμοκρασία σε βαθμούς Κελσίου αντιστοιχεί στο απόλυτο μηδέν σε Kelvin (0 K). Από αυτόν τον ορισμόη φυσική έννοια της απόλυτης θερμοκρασίας ακολουθεί: είναι ένα μέτρο της κινητικής ενέργειας των σωματιδίων που αποτελούν την ύλη, για παράδειγμα, άτομα ή μόρια.
Εκτός από την παραπάνω φυσική έννοια της απόλυτης θερμοκρασίας, υπάρχουν και άλλες προσεγγίσεις για την κατανόηση αυτής της ποσότητας. Ένα από αυτά είναι ο αναφερόμενος νόμος των αερίων του Καρόλου. Ας το γράψουμε με την εξής μορφή:
V1/T1=V2/T 2=>
V1/V2=T1/T 2.
Η τελευταία ισότητα λέει ότι σε μια ορισμένη ποσότητα ουσίας στο σύστημα (για παράδειγμα, 1 mol) και μια συγκεκριμένη πίεση (για παράδειγμα, 1 Pa), ο όγκος του αερίου καθορίζει μοναδικά την απόλυτη θερμοκρασία. Με άλλα λόγια, η αύξηση του όγκου του αερίου υπό αυτές τις συνθήκες είναι δυνατή μόνο λόγω αύξησης της θερμοκρασίας και η μείωση του όγκου υποδηλώνει μείωση της τιμής του T.
Θυμηθείτε ότι, σε αντίθεση με τη θερμοκρασία Κελσίου, η απόλυτη θερμοκρασία δεν μπορεί να είναι αρνητική.
Αρχή Avogadro και μείγματα αερίων
Εκτός από τους παραπάνω νόμους αερίων, η εξίσωση κατάστασης για ένα ιδανικό αέριο οδηγεί επίσης στην αρχή που ανακάλυψε ο Amedeo Avogadro στις αρχές του 19ου αιώνα, η οποία φέρει το επίθετό του. Αυτή η αρχή ορίζει ότι ο όγκος οποιουδήποτε αερίου σε σταθερή πίεση και θερμοκρασία καθορίζεται από την ποσότητα της ουσίας στο σύστημα. Ο αντίστοιχος τύπος μοιάζει με αυτό:
n/V=const όταν P, T=const.
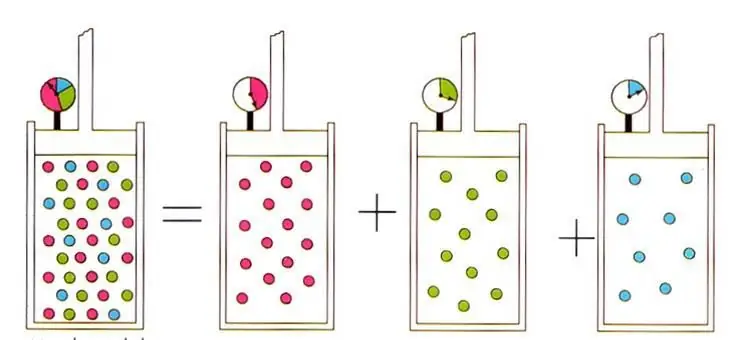
Η γραπτή έκφραση οδηγεί στον πολύ γνωστό στη φυσική των ιδανικών αερίων νόμο του D alton για τα μείγματα αερίων. Αυτόο νόμος λέει ότι η μερική πίεση ενός αερίου σε ένα μείγμα καθορίζεται μοναδικά από το ατομικό του κλάσμα.
Παράδειγμα επίλυσης προβλημάτων
Σε ένα κλειστό δοχείο με άκαμπτα τοιχώματα που περιέχει ένα ιδανικό αέριο, ως αποτέλεσμα της θέρμανσης, η πίεση αυξήθηκε κατά 3 φορές. Είναι απαραίτητο να προσδιοριστεί η τελική θερμοκρασία του συστήματος εάν η αρχική του τιμή ήταν 25 oC.
Πρώτα, ας μετατρέψουμε τη θερμοκρασία από βαθμούς Κελσίου σε Kelvin, έχουμε:
T=25 + 273, 15=298, 15 K.
Δεδομένου ότι τα τοιχώματα του αγγείου είναι άκαμπτα, η διαδικασία θέρμανσης μπορεί να θεωρηθεί ισοχορική. Για αυτήν την περίπτωση, εφαρμόζουμε τον νόμο Gay-Lussac, έχουμε:
P1/T1=P2/T 2=>
T2=P2/P1T 1.
Έτσι, η τελική θερμοκρασία προσδιορίζεται από το γινόμενο της αναλογίας πίεσης και της αρχικής θερμοκρασίας. Αντικαθιστώντας τα δεδομένα με ισότητα, παίρνουμε την απάντηση: T2=894,45 K. Αυτή η θερμοκρασία αντιστοιχεί σε 621,3 oC.






