Κατά τη μελέτη της συμπεριφοράς των αερίων στη φυσική, δίνεται μεγάλη προσοχή στις ισοδιεργασίες, δηλαδή σε τέτοιες μεταβάσεις μεταξύ των καταστάσεων του συστήματος, κατά τις οποίες διατηρείται μία θερμοδυναμική παράμετρος. Ωστόσο, υπάρχει μια μετάβαση αερίου μεταξύ κρατών, η οποία δεν είναι ισοδιεργασία, αλλά παίζει σημαντικό ρόλο στη φύση και την τεχνολογία. Αυτή είναι μια αδιαβατική διαδικασία. Σε αυτό το άρθρο, θα το εξετάσουμε με περισσότερες λεπτομέρειες, εστιάζοντας στο τι είναι ο αδιαβατικός εκθέτης αερίου.
Αδιαβατική διεργασία
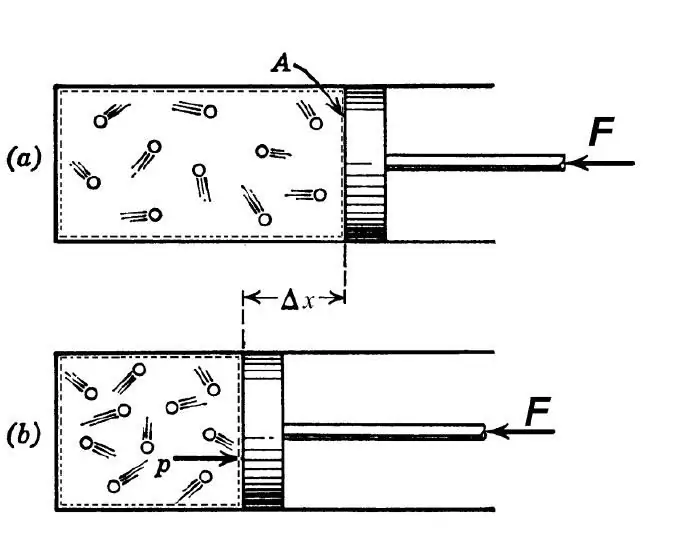
Σύμφωνα με τον θερμοδυναμικό ορισμό, ως αδιαβατική διαδικασία νοείται μια τέτοια μετάβαση μεταξύ της αρχικής και της τελικής κατάστασης του συστήματος, ως αποτέλεσμα της οποίας δεν υπάρχει ανταλλαγή θερμότητας μεταξύ του εξωτερικού περιβάλλοντος και του υπό μελέτη συστήματος. Μια τέτοια διαδικασία είναι δυνατή υπό τις ακόλουθες δύο προϋποθέσεις:
- θερμική αγωγιμότητα μεταξύ του εξωτερικού περιβάλλοντος καιτο σύστημα είναι χαμηλό για τον ένα ή τον άλλο λόγο;
- η ταχύτητα της διαδικασίας είναι υψηλή, επομένως η ανταλλαγή θερμότητας δεν προλαβαίνει να πραγματοποιηθεί.
Στη μηχανική, η αδιαβατική μετάβαση χρησιμοποιείται τόσο για τη θέρμανση του αερίου κατά την απότομη συμπίεσή του όσο και για την ψύξη του κατά τη διάρκεια της ταχείας διαστολής. Στη φύση, η εν λόγω θερμοδυναμική μετάβαση εκδηλώνεται όταν μια μάζα αέρα ανεβαίνει ή πέφτει από μια πλαγιά. Τέτοια σκαμπανεβάσματα οδηγούν σε αλλαγή του σημείου δρόσου στον αέρα και τη βροχόπτωση.
Εξίσωση Poisson για το αδιαβατικό ιδανικό αέριο

Ιδανικό αέριο είναι ένα σύστημα στο οποίο τα σωματίδια κινούνται τυχαία με υψηλές ταχύτητες, δεν αλληλεπιδρούν μεταξύ τους και είναι αδιάστατα. Ένα τέτοιο μοντέλο είναι πολύ απλό όσον αφορά τη μαθηματική του περιγραφή.
Σύμφωνα με τον ορισμό μιας αδιαβατικής διεργασίας, η ακόλουθη έκφραση μπορεί να γραφτεί σύμφωνα με τον πρώτο νόμο της θερμοδυναμικής:
dU=-PdV.
Με άλλα λόγια, ένα αέριο, που διαστέλλεται ή συστέλλεται, λειτουργεί PdV λόγω αντίστοιχης αλλαγής στην εσωτερική του ενέργεια dU.
Στην περίπτωση ενός ιδανικού αερίου, αν χρησιμοποιήσουμε την εξίσωση της κατάστασης (νόμος Clapeyron-Mendeleev), μπορούμε να πάρουμε την ακόλουθη έκφραση:
PVγ=συνεχ.
Αυτή η ισότητα ονομάζεται εξίσωση Poisson. Οι άνθρωποι που είναι εξοικειωμένοι με τη φυσική των αερίων θα παρατηρήσουν ότι εάν η τιμή του γ είναι ίση με 1, τότε η εξίσωση Poisson θα εισέλθει στον νόμο Boyle-Mariotte (ισοθερμικήεπεξεργάζομαι, διαδικασία). Ωστόσο, ένας τέτοιος μετασχηματισμός των εξισώσεων είναι αδύνατος, αφού το γ για κάθε τύπο ιδανικού αερίου είναι μεγαλύτερο από ένα. Η ποσότητα γ (γάμα) ονομάζεται αδιαβατικός δείκτης ενός ιδανικού αερίου. Ας ρίξουμε μια πιο προσεκτική ματιά στη φυσική του σημασία.
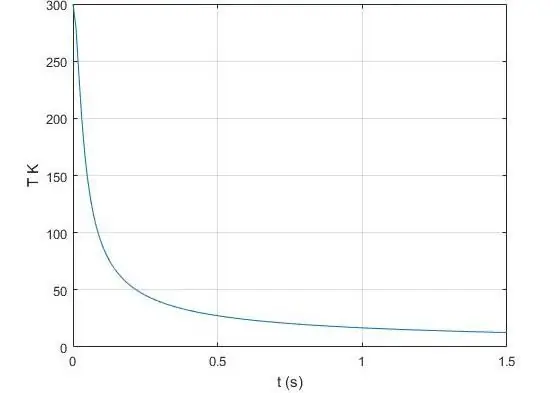
Τι είναι ο αδιαβατικός εκθέτης;
Ο εκθέτης γ, που εμφανίζεται στην εξίσωση Poisson για ένα ιδανικό αέριο, είναι ο λόγος της θερμοχωρητικότητας σε σταθερή πίεση προς την ίδια τιμή, αλλά ήδη σε σταθερό όγκο. Στη φυσική, η θερμοχωρητικότητα είναι η ποσότητα θερμότητας που πρέπει να μεταφερθεί ή να ληφθεί από ένα δεδομένο σύστημα προκειμένου αυτό να αλλάξει τη θερμοκρασία του κατά 1 Kelvin. Θα συμβολίσουμε την ισοβαρική θερμοχωρητικότητα με το σύμβολο CP και την ισοχωρική θερμοχωρητικότητα με το σύμβολο CV. Τότε ισχύει η ισότητα για το γ:
γ=CP/CV.
Δεδομένου ότι το γ είναι πάντα μεγαλύτερο από ένα, δείχνει πόσες φορές η ισοβαρική θερμοχωρητικότητα του συστήματος αερίων που μελετήθηκε υπερβαίνει το παρόμοιο ισοχορικό χαρακτηριστικό.
Θερμικές ικανότητες CP και CV
Για να προσδιορίσουμε τον αδιαβατικό εκθέτη, θα πρέπει να κατανοήσουμε καλά τη σημασία των μεγεθών CP και CV. Για να γίνει αυτό, θα πραγματοποιήσουμε το ακόλουθο σκεπτικό πείραμα: φανταστείτε ότι το αέριο βρίσκεται σε ένα κλειστό σύστημα σε ένα δοχείο με συμπαγή τοιχώματα. Εάν το δοχείο θερμανθεί, τότε όλη η μεταδιδόμενη θερμότητα ιδανικά θα μετατραπεί στην εσωτερική ενέργεια του αερίου. Σε μια τέτοια περίπτωση, η ισότητα θα ισχύει:
dU=CVdT.
ΑξίαΤο CVορίζει την ποσότητα θερμότητας που πρέπει να μεταφερθεί στο σύστημα για να θερμανθεί ισοχορικά κατά 1 K.
Τώρα ας υποθέσουμε ότι το αέριο βρίσκεται σε δοχείο με κινούμενο έμβολο. Κατά τη διαδικασία θέρμανσης ενός τέτοιου συστήματος, το έμβολο θα κινηθεί, διασφαλίζοντας ότι διατηρείται σταθερή πίεση. Δεδομένου ότι η ενθαλπία του συστήματος σε αυτή την περίπτωση θα είναι ίση με το γινόμενο της ισοβαρικής θερμοχωρητικότητας και της μεταβολής της θερμοκρασίας, ο πρώτος νόμος της θερμοδυναμικής θα λάβει τη μορφή:
CPdT=CVdT + PdV.
Από εδώ μπορεί να φανεί ότι CP>CV, αφού στην περίπτωση ισοβαρικής αλλαγής καταστάσεων είναι απαραίτητο να ξοδεύουν θερμότητα όχι μόνο για να αυξήσουν τη θερμοκρασία του συστήματος, και συνεπώς την εσωτερική του ενέργεια, αλλά και το έργο που εκτελείται από το αέριο κατά τη διάρκεια της διαστολής του.
Η τιμή του γ για ένα ιδανικό μονοατομικό αέριο
Το απλούστερο σύστημα αερίου είναι ένα μονατομικό ιδανικό αέριο. Ας υποθέσουμε ότι έχουμε 1 mol τέτοιου αερίου. Θυμηθείτε ότι στη διαδικασία ισοβαρικής θέρμανσης 1 mol αερίου μόνο κατά 1 Kelvin, λειτουργεί πράγματι ίσο με το R. Αυτό το σύμβολο χρησιμοποιείται συνήθως για να δηλώσει την καθολική σταθερά αερίου. Είναι ίσο με 8, 314 J / (molK). Εφαρμόζοντας την τελευταία έκφραση της προηγούμενης παραγράφου για αυτήν την περίπτωση, παίρνουμε την ακόλουθη ισότητα:
CP=CV+ R.
Από όπου μπορείτε να προσδιορίσετε την τιμή της ισοχορικής θερμοχωρητικότητας CV:
γ=CP/CV;
CV=R/(γ-1).
Είναι γνωστό ότι για έναν σπίλομονοατομικό αέριο, η τιμή της ισοχωρικής θερμοχωρητικότητας είναι:
CV=3/2R.
Από τις δύο τελευταίες ισότητες ακολουθεί η τιμή του αδιαβατικού εκθέτη:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Σημειώστε ότι η τιμή του γ εξαρτάται αποκλειστικά από τις εσωτερικές ιδιότητες του ίδιου του αερίου (από την πολυατομική φύση των μορίων του) και δεν εξαρτάται από την ποσότητα της ουσίας στο σύστημα.
Εξάρτηση του γ από τον αριθμό των βαθμών ελευθερίας
Η εξίσωση για την ισοχωρική θερμοχωρητικότητα ενός μονατομικού αερίου γράφτηκε παραπάνω. Ο συντελεστής 3/2 που εμφανίστηκε σε αυτό σχετίζεται με τον αριθμό των βαθμών ελευθερίας σε ένα άτομο. Έχει την ικανότητα να κινείται μόνο σε μία από τις τρεις κατευθύνσεις του χώρου, δηλαδή υπάρχουν μόνο μεταφραστικοί βαθμοί ελευθερίας.
Αν το σύστημα σχηματίζεται από διατομικά μόρια, τότε προστίθενται δύο ακόμη περιστροφικές μοίρες στις τρεις μεταφορικές. Επομένως, η έκφραση για CV γίνεται:
CV=5/2R.
Τότε η τιμή του γ θα είναι:
γ=7/5=1, 4.
Σημειώστε ότι το διατομικό μόριο έχει στην πραγματικότητα έναν ακόμη βαθμό δόνησης, αλλά σε θερμοκρασίες αρκετών εκατοντάδων Kelvin δεν ενεργοποιείται και δεν συμβάλλει στη θερμική ικανότητα.
Αν τα μόρια αερίου αποτελούνται από περισσότερα από δύο άτομα, τότε θα έχουν 6 βαθμούς ελευθερίας. Ο αδιαβατικός εκθέτης σε αυτήν την περίπτωση θα είναι ίσος με:
γ=4/3 ≈ 1, 33.
ΛοιπόνΈτσι, όσο αυξάνεται ο αριθμός των ατόμων σε ένα μόριο αερίου, η τιμή του γ μειώνεται. Εάν δημιουργήσετε ένα αδιαβατικό γράφημα στους άξονες P-V, θα παρατηρήσετε ότι η καμπύλη για ένα μονοατομικό αέριο θα συμπεριφέρεται πιο έντονα από ότι για ένα πολυατομικό.
Αδιαβατικός εκθέτης για ένα μείγμα αερίων
Δείξαμε παραπάνω ότι η τιμή του γ δεν εξαρτάται από τη χημική σύσταση του συστήματος αερίων. Ωστόσο, εξαρτάται από τον αριθμό των ατόμων που αποτελούν τα μόριά του. Ας υποθέσουμε ότι το σύστημα αποτελείται από Ν στοιχεία. Το ατομικό κλάσμα του συστατικού i στο μείγμα είναι ai. Στη συνέχεια, για να προσδιορίσετε τον αδιαβατικό εκθέτη του μείγματος, μπορείτε να χρησιμοποιήσετε την ακόλουθη έκφραση:
γ=∑i=1N(aiγ i).
Όπου γi είναι η τιμή γ για το i-ο στοιχείο.
Για παράδειγμα, αυτή η έκφραση μπορεί να χρησιμοποιηθεί για τον προσδιορισμό του γ του αέρα. Δεδομένου ότι αποτελείται από 99% διατομικά μόρια οξυγόνου και αζώτου, ο αδιαβατικός δείκτης του θα πρέπει να είναι πολύ κοντά στην τιμή του 1,4, κάτι που επιβεβαιώνεται από τον πειραματικό προσδιορισμό αυτής της τιμής.






